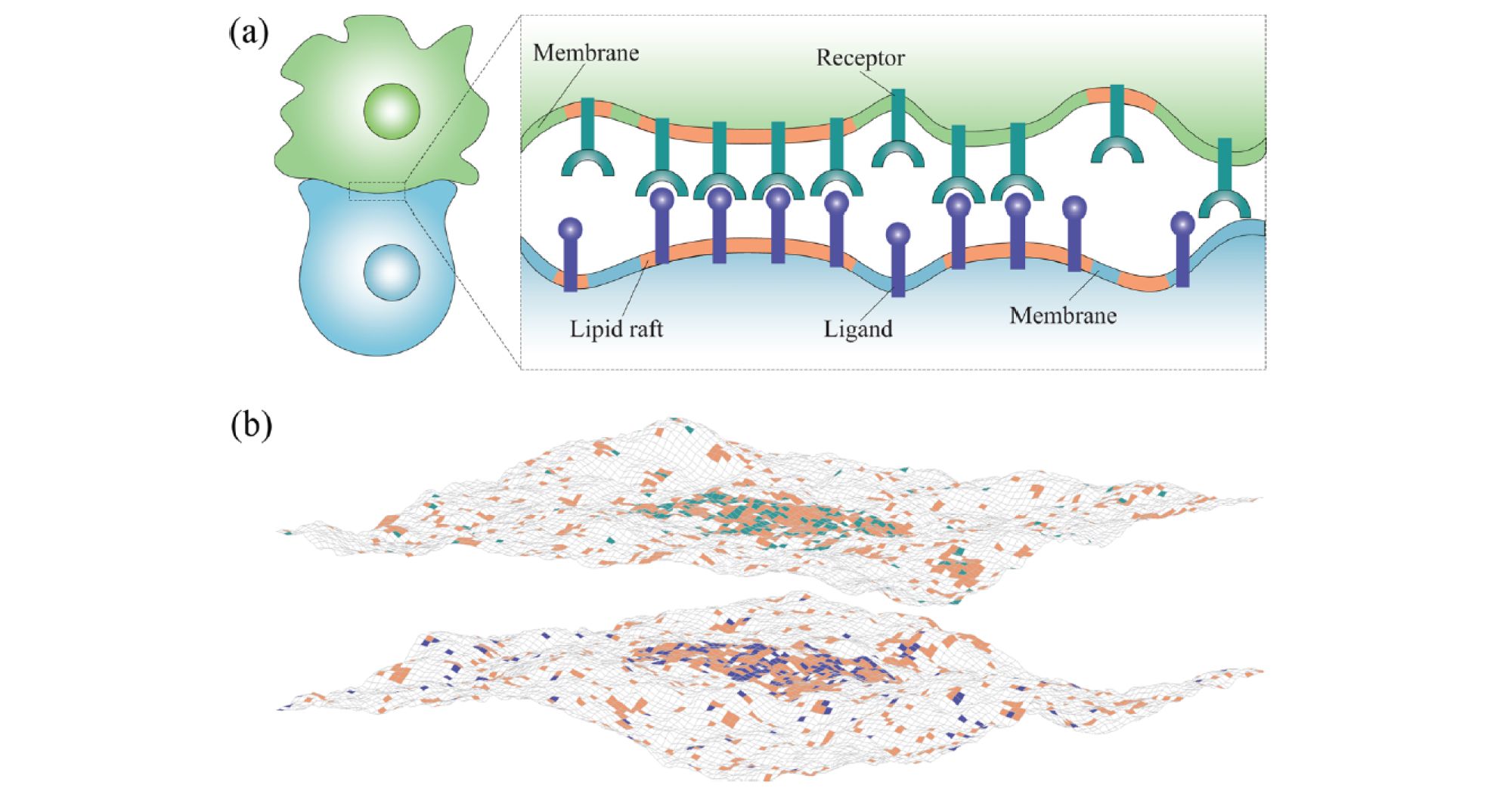
Komórki biologiczne muszą rozpoznawać ogromną ilość różnych substancji oraz sąsiednich komórek. Dlatego wiele zróżnicowanych cząsteczek na powierzchni komórki pełni funkcje receptorów, które wykrywają różnorodne cząsteczki w otoczeniu komórki i przekazują odpowiednie informacje do wnętrza komórki.
Niektóre z tych receptorów łączą się z tzw. tratwami lipidowymi, które są małymi (o średnicy od 10 do 200 nm), wzbogaconymi w cholesterol obszarami w błonie otaczającej komórkę. Jednym z istotnych problemów współczesnej biofizyki jest zrozumienie w jaki sposób owe tratwy lipidowe wraz ze stowarzyszonymi z nimi receptorami reagują na różne bodźce i czynniki, a w szczególności na fizyczny kontakt jednej komórki biologicznej z inną (rys. 1).
Używając zaawansowanych metod fizyki statystycznej i obliczeniowej, naukowcy z Instytutu Fizyki PAN we współpracy z naukowcami z Chińskiej Akademii Nauk oraz Uniwersytetu w Nanjing zbadali wpływ kontaktów międzykomórkowych na stabilność i rozmiary tratw lipidowych. Wyniki ich badań opublikowane w czasopiśmie Nano Letters [1] wyjaśniają, w jaki sposób tworzenie kontaktów międzykomórkowych prowadzi do agregacji receptorów stowarzyszonych z tratwami lipidowymi. Na efekt ten mają wpływ zarówno mechaniczne własności błon komórkowych (np. sztywność błony na zginanie) jak i siła niekowalencyjnych wiązań tworzących kontakty międzykomórkowe.
Agregacja receptorów, czyli nagromadzenie receptorów w pewnych obszarach na powierzchni komórki, może prowadzić do wyzwolenia określonych reakcji komórki na dany bodziec. Jak podkreśla dr hab. Bartosz Różycki z Instytutu Fizyki PAN, wyniki badań opublikowane przez naukowców z Chin i Polski [1] wnoszą duży wkład do zrozumienia fizycznych mechanizmów wyzwalania reakcji komórki na skutek kontaktów międzykomórkowych, np. w procesie rozróżniania komórek "własnych" od "obcych" przez limfocyty wchodzące w skład układu odpornościowego. Wyniki te mogą przyczynić się między innymi do projektowania nowych immunoterapii.
Opisane badania były wspierane w Polsce przez Narodowe Centrum Nauki poprzez grant No. 2016/21/B/NZ1/00006.
[1] "Intercellular receptor-ligand binding and thermal fluctuations facilitate receptor aggregation in adhering membranes",
Long Li, Jinglei Hu, Bartosz Różycki and Fan Song, Nano Letters 20, 722-728 (2020)